2019 年首个诺贝尔奖公布,让细胞缺氧来治疗癌症

昨(7)日下午5点30分,诺贝尔委员会公布了今年的诺贝尔生理学或医学奖得主,奖项颁发给来自美、英的三位科学家,以表彰他们对于细胞是怎么感知并适应氧气变化的发现,其研究「细胞如何适应氧气供应量的变化」为贫血、癌症、其他疾病的新治疗策略打开新大门。
他们分别是来自哈佛医学院达纳-法伯癌症研究所的William G. Kaelin, Jr.,牛津大学和弗朗西斯·克里克研究所的Peter J. Ratcliffe,以及美国约翰霍普金斯大学医学院的Gregg L. Semenza。他们将平分900万瑞典克朗(约合人民币647万元)的奖金。
氧气对地球上所有生物都是至关重要的元素,几乎所有动物体内细胞的粒线体,都利用氧气才能将食物转化为能量,但长期以来,科学家们并不清楚细胞如何去适应体内氧气值的变化。
而美国癌症学家威廉·乔治·凯林(William George Kaelin)、英国分子生物学家彼得·拉特克利夫(Sir Peter J. Ratcliffe)、美国医学家格雷格·塞门扎(Gregg L. Semenza)3 人,发现了细胞如何感应与适应氧气供应不断变化的关键分子机制,可以调节基因活性去应对不同的氧气量。
过去,科学家已知颈动脉体(carotid body)含有一种能侦测血液氧含量的特定细胞,比利时医学家柯奈尔‧海门斯并发现了血氧如何透过颈动脉体来控制呼吸频率,荣获 1938 年诺贝尔生医奖。
不过除了颈动脉体可快速适应缺氧环境外,还有其他生理机制也参与其中,另一个关键是称为「红血球生成素(Erythropoietin,EPO)」的糖蛋白激素浓度升高,会增加红血球生成量以提高携氧量,但科学家还不清楚氧本身如何控制这道过程。
格雷格·塞门扎和彼得·拉特克利夫于是分别投入了 EPO 基因的研究。在经过基因编辑的小鼠实验中,格雷格·塞门扎发现位于 EPO 基因旁的特定 DNA 片段直接介入了缺氧反应,为理解这种介入缺氧反应的细胞成分,格雷格·塞门扎又培养了肝细胞,并从中发现一种称为缺氧诱导因子(hypoxia-inducible factor,HIF)的蛋白质复合物,会与上述特定 DNA 片段结合。
1995 年时,格雷格·塞门扎发表了鉴定编码 HIF 的基因研究,发现了编码缺氧诱导因子-1α(HIF-1α)的一对 DNA 结合蛋白(DNA-binding protein),当体内氧含量极高时,细胞中几乎不含 HIF-1α;当体内氧气含量低时,HIF-1α 含量就会增加,结合并调节 EPO 基因或其他具有 HIF 结合 DNA 片段的基因。
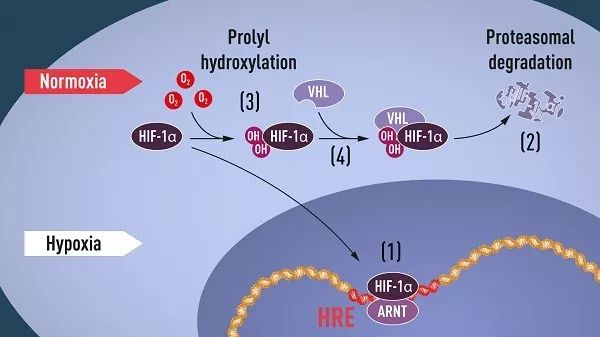
在缺氧环境下,HIF-1α 通常不容易被降解,而在正常含氧量下,HIF-1α 则会迅速被一种称为泛素(ubiquitin)的小蛋白标记、接着被蛋白酶体(Proteasomes)降解,科学家们好奇泛素如何透过氧依赖性方式结合 HIF-1α。
同一时间,威廉·乔治·凯林正在研究林道症候群(von Hippel–Lindau,VHL),已知这种疾病会增加罹患某些癌症的风险。凯林发现,无功能性 VHL 基因的细胞会响应缺氧环境,接着格雷格·塞门扎团队又发现,VHL 蛋白与 HIF 的一种成分会相互作用,一旦氧含量升高就将后者标记为「准备破坏的对象」,从而关闭细胞对缺氧的反应。
这些研究让我们更加了解氧含量如何调节基本的生理过程,并也为贫血、癌症或其他疾病带来另一种治疗方向。
来源:科技新报
推荐阅读


 扫一扫下载订阅号助手,用手机发文章
扫一扫下载订阅号助手,用手机发文章 
朋友会在“发现-看一看”看到你“在看”的内容