戳穿热胀冷缩的真相
以下文章来源于费米科学 ,作者小虾
上知天文,下知物理,中通化学,还知道怎么变美!我们要让天下没有难懂的科学,约吗?


○“冰山一角”
这张流传甚广的图片很多人都见过,漂浮在海面上的冰山,露出水面的只是一小部分,绝大部分藏在水下。
原因其实很简单:冰的密度比水小一点点,大约是水的0.9倍,根据阿基米德浮力定律,冰会漂浮在水面上,90%的体积在水下,10%的体积露出水面。
可是,你有没有想过:
 这正常吗
这正常吗
在我们的生活经验中,“热胀冷缩”是一个普遍成立的规律。就算发生了物态变化,也依然成立。一般情况下,物质有三态:
固、液、气
物质的形态取决于组成它的分子聚集在一起的形态。分子之所以会聚集在一起,是因为它们之间有相互吸引的力(注意!不是万有引力,而是一种电磁力!)。
而所谓的“热”,实际上是分子的无规则运动,分子运动得越剧烈,就越容易摆脱分子间吸引力的束缚,变得更稀疏。热胀冷缩缘于此,物态变化也缘于此,只是二者一个是量变,一个是质变。

○物质的三态
组成固态物质的分子十分乖巧,它们手拉着手,紧密而整齐地排列着。每个分子有固定的位置,只能在自己的位置附近作小范围的振动。
把固体物质加热到它的熔点,分子的振动变得非常剧烈。如果继续加热,大部分分子都会松手,队形变得散漫,分子可以相对自由地移动。但分子间的吸引力仍起作用,它们仍然聚在一起。这就是液态。
当液体的温度达到沸点,如果继续加热,分子们就会彻底摆脱分子间吸引力的束缚,彼此远离,各自乱飞,这就是气态。
一般的物质从固态变为液态,体积会增大一点点;从液态变成气态,体积会增大1000倍左右。相应地,密度就是:固>液>气。
或者说,热胀冷缩在物态变化时依然成立。
所以
一般情况下
同种物质固液共存时
固体会沉没在液体底部
冰就是固态的水,但密度却比液态水小,漂浮在水面上。
世上的物质千千万,水却偏偏是个“热缩冷胀”的奇葩。
但是再回过头来想想:
正常的物质固液共存,

没见过就对了。
正是因为地球上充满了水这种不正常的物质,生命才得以生存。
如果冰的密度比水大,会怎样?
每到冬天
江河湖泊从下往上结冰
水的表面没有冰层隔热
水体最终会全部冻结
水里的生物(包括小虾)全部冻死



我们应当庆幸,水是个异类。
那么,
 是为什么
是为什么
前面说过,物质处于固态的时候,分子手拉着手,排列紧密……
但是水分子有个特点:
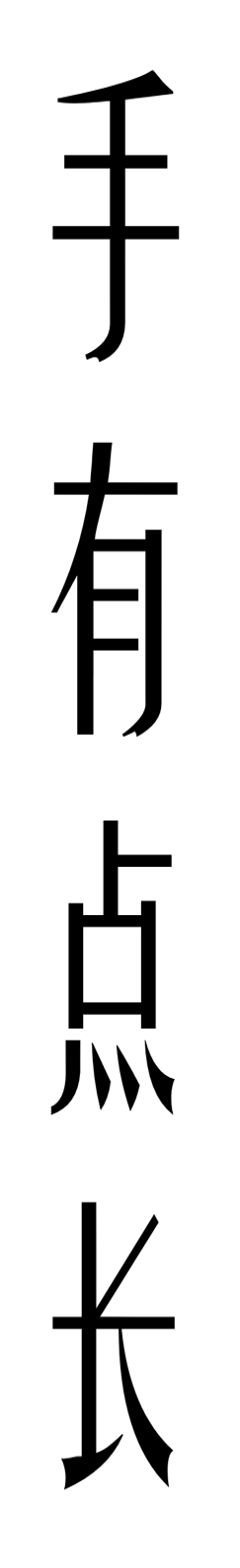
所以,对于水分子来说,手拉手排好队反而是比较稀疏的阵型,散漫地堆成一团才更紧密。就像这样:
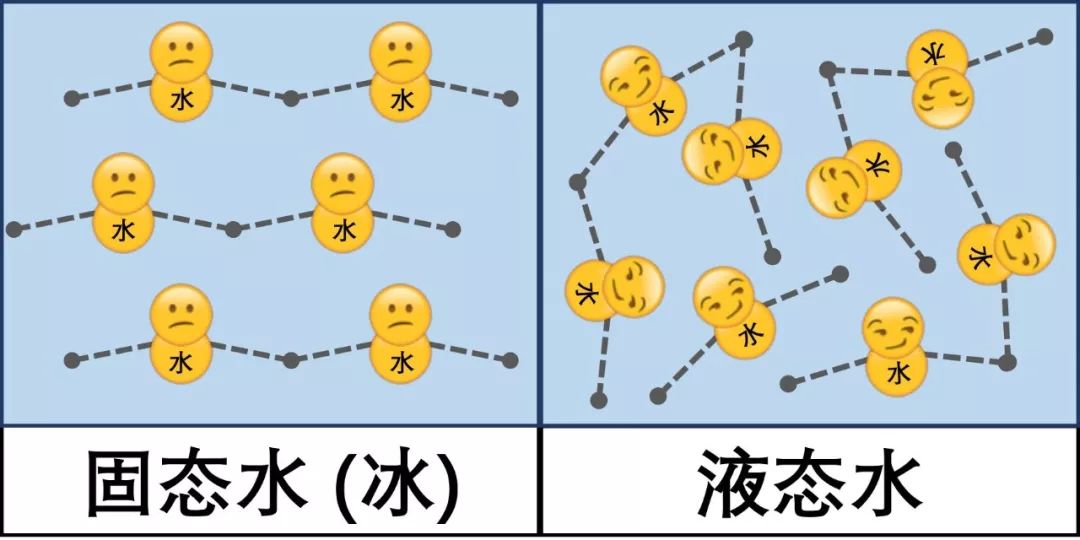
○冰和水的分子聚集形态示意图。
水的分子式是
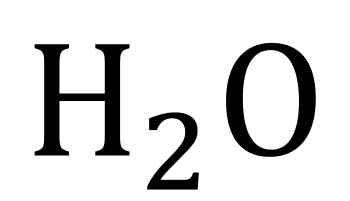
水分子由2个氢 (H) 原子和1个氧 (O) 原子组成,形状类似于一个米老鼠的头。
水分子之间有一种特殊的结合方式,也就是那有点长的手,叫做:
氢键
水分子中的氢原子和相邻水分子的氧原子之间可以形成氢键。想象一个水分子的2个氢原子各“发出”1根氢键,它的氧原子又能“接受”2根氢键,所以每个水分子最多可以通过氢键与周围4个水分子结合。
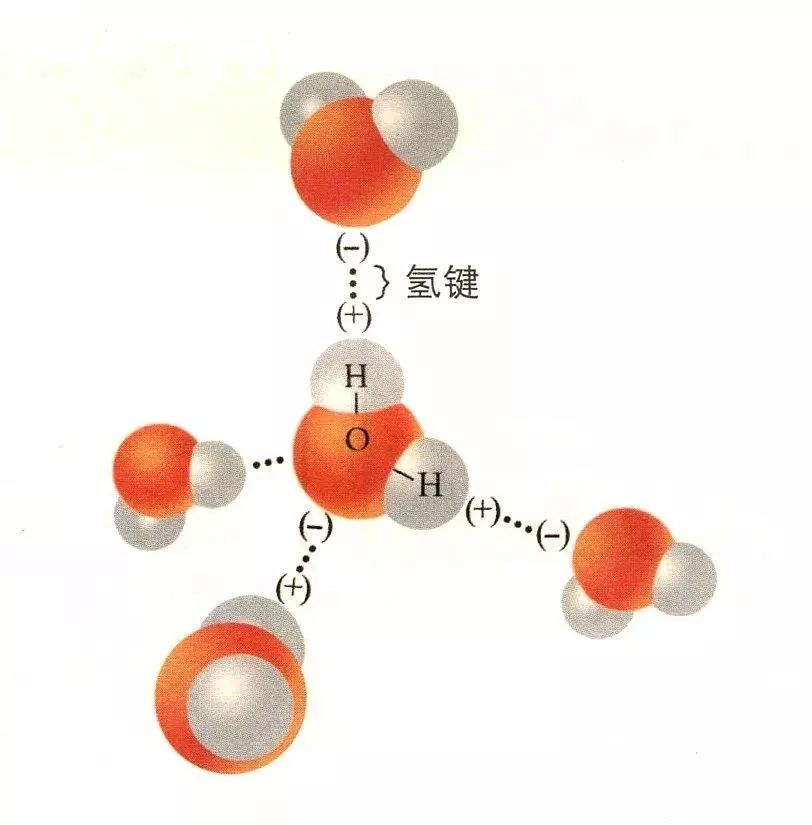
○水分子之间的氢键
与一般的分子间作用力不同的是,氢键有确定的长度和角度,它将水分子结合在一起的同时也限制了水分子相互靠近。
固态水内部所有的水分子都用上了全部4根氢键,组成低密度的四面体结构。而液态水中的水分子通常都只有1个或2个氢键,组成高密度的无序结构。这就解释了为什么冰的密度比水小。
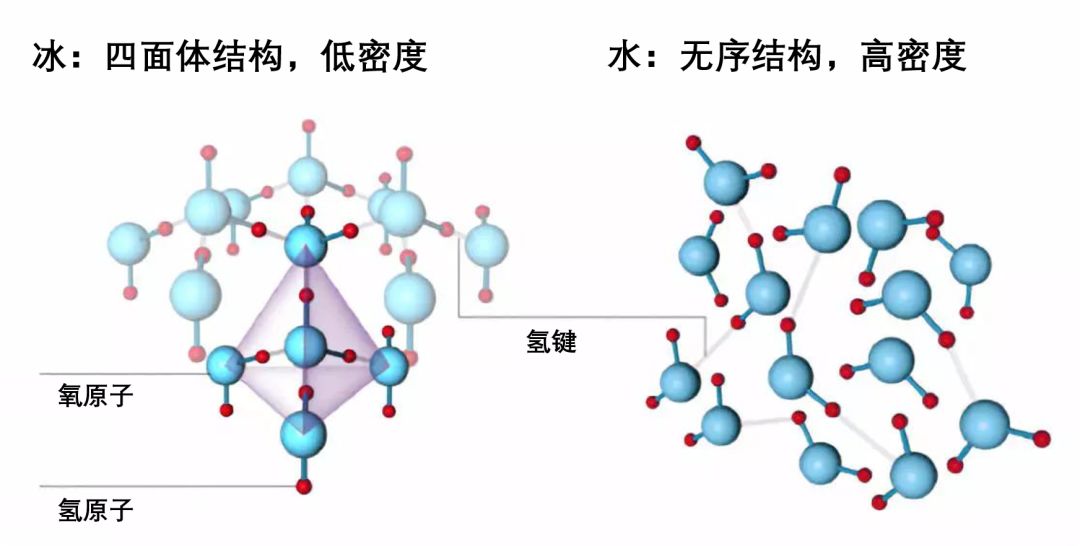
○水的低密度四面体结构,和高密度无序结构
实际上水的反常膨胀不仅仅发生在结冰的时候。水在4℃时密度最大,低于4℃的水就有“热缩冷胀”的性质。
有科学家认为,液态水中可能也存在以上两种结构的水分子集团,它们在不停地相互转化,达到平衡。而降温会增加水中的氢键,从而增加低密度四面体结构的占比,造成液态水的反常膨胀。
但是,水在0℃就要结冰了。0℃~4℃这个温度范围太小,很难将液态水的反常膨胀性质研究透。所以,需要借助液体普遍具有的“过冷现象”,将水的温度降到0℃以下。
过冷现象
如果液体足够纯净,且在降温时没有受到外界的扰动,是有可能达到低于凝固点的温度却不凝固的,但是一旦受到外界的扰动,就会快速凝固。这种现象叫做液体的“过冷”。

○用拳击让一瓶过冷水快速结冰。获得过冷水的方法是:将一瓶处于室温的纯净水放入冰箱冷冻室静置2~3小时,然后小心地将其取出。
有实验现象表明,过冷水持续降温时,也会持续地反常膨胀,同时也出现越来越大的密度起伏。正常的物质应该是温度越低,密度起伏越小才对。
所以这可能说明过冷的液态水中确实存在2种不同结构的水分子集团,或者说两种不同的物态:像水的高密度水、和像冰的低密度水。
而如果不停地降低温度,或许最终会使得这两种水彻底分开。
但是这个过程很难实现,因为温度很低的时候,水实在太容易结冰……

2018年3月,荷兰阿姆斯特丹大学的桑德·沃特森(Sander Woutersen)用一种结构与水类似的防冻剂阻止水结冰,同时保持水的其他性质不变。
他们将混合溶液的温度降至-100℃以下,在冷却的过程中,混合溶液的密度发生了突变。于是他们认为这证明了液态水存在两种不同的状态。
也就是说
水不是一种液体
而是两种
这项工作也得到了同行的认可,但是,溶液毕竟不是纯水,真正的纯水到底是否有两种不同的状态,还有待进一步的研究。

氢键造就了水分子组合在一起的两种不同结构。它们区分了冰和水,也可能在液态水中共存。从而成就了水的奇葩性质——反常膨胀。
结冰时膨胀
在4℃以下,降温时膨胀

氢键让水千变万化,成为物质世界最特殊的存在。但也正因为只有最特殊的水才能孕育生命,我们对奇妙的水早已见怪不怪。
没有固定形状的液态水尚且有2种不同的微观结构,那么冰又有多少种结构呢?

○各式各样的雪花
世上没有两片相同的雪花,但所有雪花的微观结构都是相同的。它们的水分子都组成六边形的“晶格”,这决定了它们的宏观形状都是六边形。而所有雪花,以及自然界的绝大多数冰,都是简简单单的同一种冰。

○自然界最常见的冰的晶体结构
不过,科学家们在实验室里,通过改变温度、压强等等的一系列骚操作,发现了至少18种冰!
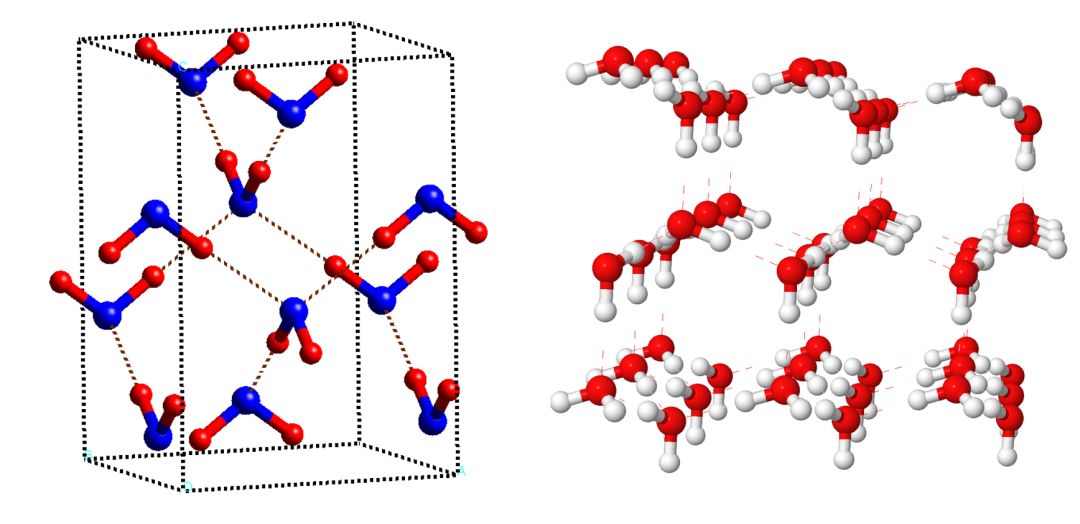
○另外两种不同的冰,你发现它们与普通冰的差别了吗?
据说没人知道还有多少种冰在等着被发现,你呢?

来源:费米科学
编辑:小烩饼
