背后的故事——喜树碱
以下文章来源于药物递送 ,作者石攻玉
专注药物递送技术和高端制剂,分享相关知识,做一个有态度、有温度、有深度的公众号,愿分享的内容对你有所帮助。
2022年4月15日,施维雅公司(SERVIER)宣布,盐酸伊立替康脂质体注射液获得中国国家药品监督管理局(NMPA)正式批准,与5-氟尿嘧啶(5-FU)和亚叶酸(LV)联合用于治疗接受吉西他滨治疗后进展的转移性胰腺癌患者。喜树碱类药物作为广谱的抗肿瘤药物,目前已有多款产品应用于临床。
文丨石攻玉

喜树碱的起源



喜树碱(Camptothecin,CPT)为吡咯喹啉细胞毒性生物碱,是除紫杉醇之外研究最多的天然抗肿瘤药物之一,存在于在我国特有的珙桐科植物喜树的果实或根中。《浙江民间常用草药》中记载,喜树的根皮具有清热解毒,散结消肿之功效,果实具有活血化瘀之功效,常用来煎汤内服或者是研末吞服,治疗牛皮癣、疮肿等症状。
1966年,美国国家癌症研究所的Monreoe E. Wall 和Mansukh C. Wani 从原产于中国中部的喜树树皮和树干中分离得到一种五环单萜生物碱,这是对喜树碱的最早研究。
1967年到1970年,研究者发现该五环单萜生物碱在体外对Hela细胞(宫颈癌细胞的细胞系)、L1210细胞(小鼠淋巴细胞白血病细胞)及啮齿类动物显示出较强的抗肿瘤活性,同时还表明对胃癌、直肠癌和白血病等多种恶性肿瘤均有一定的疗效,这引发了科学界对植物喜树和喜树碱类化合物的研究热潮,陆陆续续发现了更多的喜树碱类化合物。但因多种原因,喜树碱药物的临床应用却未取得有效推进。
1985年,Hsiang和其同事发现喜树碱及其衍生物是以拓扑异构酶I(Topoisomerase I,Topo I)为靶点,通过TopoI-DNA可裂解复合物可逆结合,形成的CPT-Topo I-DNA三元复合物可抑制DNA的复制和转录,进而导致癌细胞的死亡。相比TopoII抑制剂,Topo I抑制剂疗效高,抗瘤谱广,喜树碱对拓扑异构酶I有专一抑制性,引发了新一轮的关注。
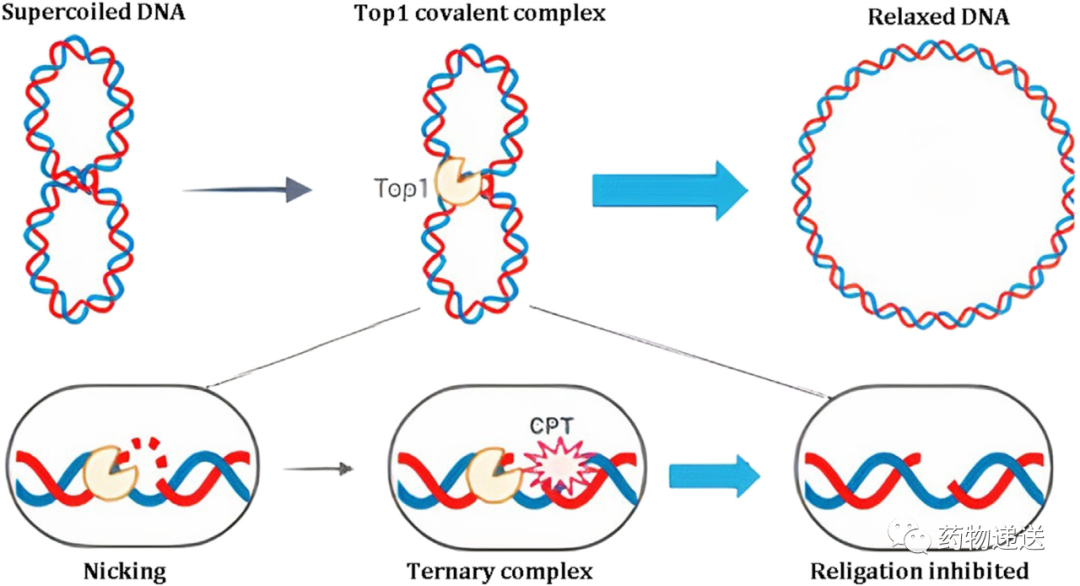
图1 喜树碱的药理作用示意图

喜树碱药物的开发



喜树碱为不溶于酸不溶于水的中性生物碱,也很难溶于一般的有机溶剂。对光和热敏感,光照会影响喜树碱的吸光度,避光则保持稳定,而加热则会使喜树碱分解。室温下经稀碱处理,容易开环成水溶性羧酸盐,酸化则又重新内酯化成环。缓冲盐中,pH>7.4时以开环的羧酸盐为主,与人血清白蛋白有较大的亲和力,减少细胞摄取,甚至引发严重毒副反应;pH<4.5时以内酯形式为主,具有抗肿瘤活性。临床应用中曾尝试转变为羧酸钠盐增加水溶性,但是羧酸钠盐形式的喜树碱活性低,甚至会因为从肾脏排出引发出血性膀胱炎、骨髓抑制和胃肠道毒性。
构效关系方面,喜树碱分子由A、B、C、D、E五个环骈合而成,其中A、B环为喹啉环,C环为吡咯环,D环为吡啶酮,E环为一个具有S型手性碳的α-羟基内酯。五个环间形成连续共轭体系,具有天然荧光使其对光敏感。
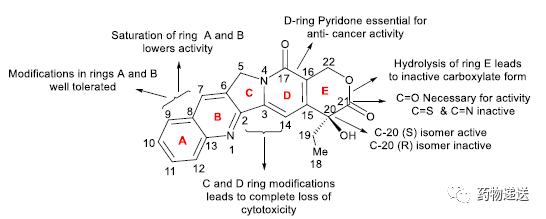
图2 喜树碱的构效关系
喜树碱类药物的开发过程中,主要存在三个问题:一是其特殊的结构导致脂溶性和水溶性都较差,没有较好的成药性,必须进行水溶性改造;二是水溶性改造会导致药物的快速释放,过高的血药浓度会引发严重的毒副作用,如腹泻,出血性膀胱炎,严重的骨髓抑制;三是结构改造需要考虑药物的释放速率和稳定性,保证有效性的同时还要考虑安全性。为获得低毒水溶性好的喜树碱衍生物,通常是对其五环骨架上某些活性位点进行修饰,例如A、B、E环,用以改善喜树碱的水溶性,降低毒副作用,增加内酯环的稳定性,其中研究最多的修饰位点是7、9、10和20位碳。
最早开始研究的衍生物是10-羟基喜树碱(10-Hydroxy camptothecin,HCPT),是由我国在20世纪70年代自主研制的抗肿瘤药物,由于其可靠的临床疗效而受到人们的广泛关注。在20世纪90年代,又成功开发了新一代喜树碱药物拓扑替康(Topotecan,TPT)和伊立替康(Irinotecan,CPT-11),之后也相继开发了很多类似的药物。
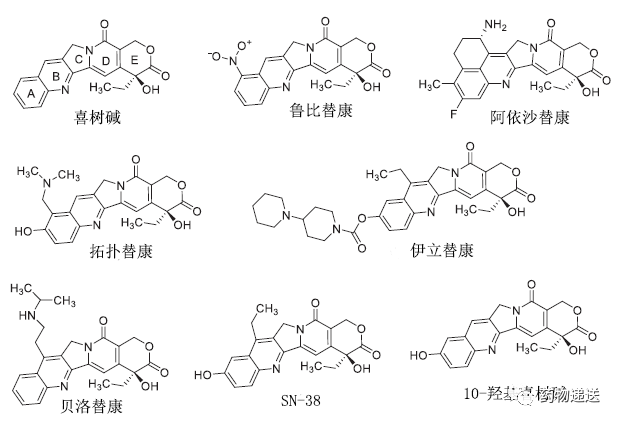
图3 喜树碱及其衍生物
1994年,伊立替康(Irinotecan,CPT-11)获FDA批准上市,用于治疗小细胞和非小细胞肺癌及宫颈癌和卵巢癌;1996年,拓扑替康(Topotecan,TPT)获FDA批准上市,用于二线治疗小细胞肺癌和卵巢癌;2005年,贝洛替康(Belotecan,CDK-602)在韩国获批上市,用于小细胞肺癌和卵巢癌的治疗。
表1 获批上市的喜树碱类药物
名称 | 上市年份 | 开发公司 | 适应症 |
伊立替康 | 1994 | 日本第一制药 | 小细胞和非小细胞肺癌及宫颈癌和卵巢癌 |
拓扑替康 | 1996 | Smithkline Beecham | 二线治疗小细胞肺癌和卵巢癌 |
贝洛替康 | 2005 | 韩国钟根堂制药 | 小细胞肺癌和卵巢癌 |

药物递送技术助力喜树碱药物



经过多年的技术积累和发展,药物递送被广泛应用于抗肿瘤领域,提高药物有效性,降低药物毒性,改善药物安全性。已有多种技术应用于喜树碱药物的开发,例如脂质体、抗体偶联药物、树枝状大分子、胶束等技术。
最成功的喜树碱脂质体药物案例是由中国台湾智擎生技制药(Pharma Engine)伊立替康脂质体(Onivyde),其商业化道路在HermesBiosci、Merrimack、Baxter、Shire、IPSEN、Servier等多家公司间授权转让,目前分别由中国台湾智擎(中国台湾地区)、Servier公司(欧亚区)及IPSEN公司(美洲区)三家公司持有。
具有广谱抗肿瘤作用的伊立替康,最早在1981年由日本学者合成,Pfizer开发上市,用于成人转移性大肠癌的治疗及一些化疗失败患者的辅助治疗,其专利已于2007年8月过期。目前国内有8家原料药供应商,上市的制剂产品有6家。
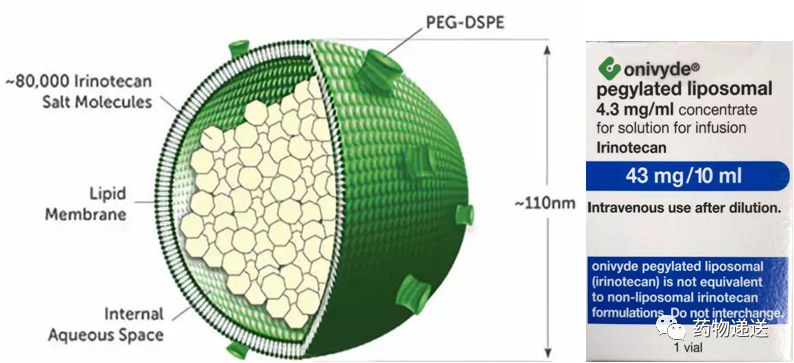
图4 伊立替康脂质体注射液
在Onivyde的生产过程中,以葡萄糖溶液溶解活性成分盐酸伊立替康三水合物,随后与空白脂质体混合孵育,通过主动载药方式将药物包载到脂质体内水相,并以伊立替康八硫酸蔗糖盐沉淀的形式存在。Onivyde以脂质体为载体,既解决了伊立替康溶解度低无法注射给药的问题,又提高了伊立替康的安全性和有效性,这个案例对其他喜树碱类药物具有非常重要的借鉴意义。
Onivyde于2015年获FDA新药上市核准,联合5-氟尿嘧啶和甲酰四氢叶酸(5-FU/LV),用于治疗既往接受吉西他滨为基础的化疗药物治疗病情进展的胰腺转移性腺癌。2020年6月,在日本获批上市,用于治疗化疗后无法切除的胰腺癌,成为全球第一个也是目前核准使用在曾接受一线标准治疗药物吉西他滨失败后的晚期转移性胰腺癌的新药。目前国内已有多家企业对伊立替康脂质体进行仿制或者改良。
表2 伊立替康脂质体(Onivyde)获批历程
国家/地区 | 获批时间 |
美国 | 2015年 |
欧洲 | 2016年 |
韩国、新加坡 | 2017年 |
日本 | 2020年 |
中国 | 2022年 |
表3 国内伊立替康脂质体进行的临床试验
产品名 | 申请人 | 临床进度 | 适应症 |
盐酸伊立替康脂质体注射液 | 南京绿叶制药 | I期 | 晚期实体肿瘤 |
II期 | 小细胞肺癌 | ||
四川科伦 | I期 | 晚期实体瘤 | |
齐鲁制药 | I期 | 实体瘤 | |
恒瑞医药 | I期 | 实体瘤 | |
III期 | 胰腺癌 | ||
伊立替康脂质体 | 艾昆纬医药 | III期 | 铂类药物治疗下/后发生进展的小细胞肺癌 |
其他药物方面,贝洛替康和SN-38(7-乙基-10-羟基喜树碱)也在开发脂质体药物。SN-38是伊立替康(本身为前体药物)经羧酸酶转化后的活性代谢物,其抑制拓扑酶I的活性远大于伊立替康。LE-SN38(Liposome-Entrapped SN38 )是Neopharm公司开发的SN-38脂质体,该产品的核心技术是采用四豆蔻酰甘油心磷脂,能与亲脂性药物紧密作用,稳定地嵌入到脂质体磷脂膜中,极大地提高体内外稳定性,同时也可以使溶解性较差的SN-38能注射给药。
将抗体通过连接子(Linker)与药物载荷(payload)连接在一起形成抗体药物偶联物(Antibody Drug Conjugates),因抗体能靶向特定抗原而被誉为能够精准靶向肿瘤细胞“生物导弹”。
戈沙妥珠单抗(Trodelvy®、Sacituzumab govitecan、IMMU-132)通过CL2A连接子将靶向癌细胞表面Trop-2的单克隆抗体hRS7和伊立替康活性代谢产物SN-38偶联形成ADC型靶化结合药物,由Immunomedics公司开发,其中hRS7为特异性靶向的人源化IgG1单克隆抗体,具有特异性强、亲和力高、稳定性好以及半衰期长的特点;CL2A连接子属于可剪切连接子;连接的小分子药物SN-38为拓扑异构酶I抑制剂,在血液中高度稳定,有效避免系统性脱靶效应。
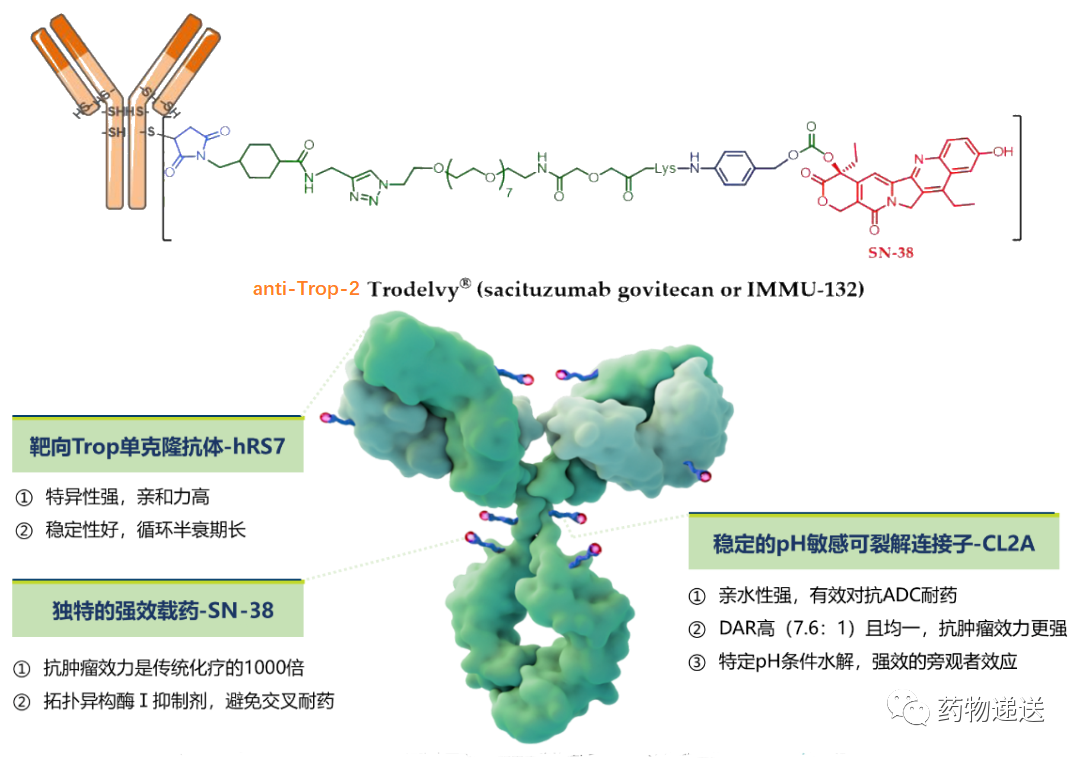
图5 戈沙妥珠单抗结构示意图及其特点
该产品设计在类似肿瘤微环境的酸性条件下中可发生水解,可以实现精准高效的载药释放以及旁观者效应,在抗体和化疗药物的双重作用下,既能精准靶向结合高表达Trop-2的肿瘤细胞,又能释放化疗药物对肿瘤进行攻击,避免引起严重的毒副作用。2020年4月22日,戈沙妥珠单抗获得FDA加速批准,用于三线及以上转移性三阴乳腺癌,成为首个上市的Trop-2靶向药物。
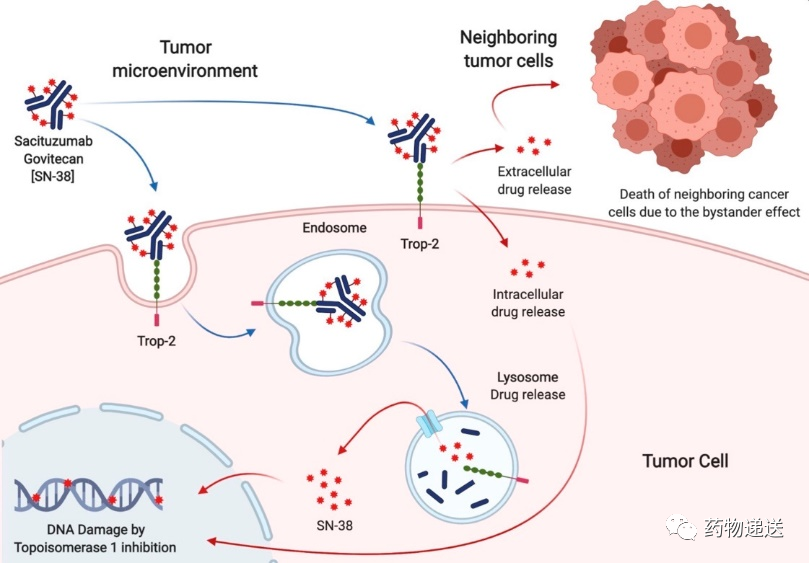
图6 戈沙妥珠单抗作用机制
另一款递送喜树碱药物的ADC是由第一三共和阿斯利康合作开发推广的DS-8201(trastuzumabderuxtecan)。该ADC药物的单克隆抗体是曲妥珠单抗(trastuzumab),连接子为4肽链间半胱氨酸,荷载的小分子药物为拓扑异构酶I抑制剂德卢替康(deruxtecan,DXd)。在连接子的作用下,DS-8201在血液中高度稳定,脱落率极低,不影响代谢速率还能保证稳定性和均一性。可裂解的连接子使DS-8201的载药释放过程简单,进入细胞后经溶酶体蛋白酶识别连接子位点并切割释放载药即可,效率更高。DS-8201可靶向递送细胞毒制剂至癌细胞内,减少细胞毒制剂的全身暴露。
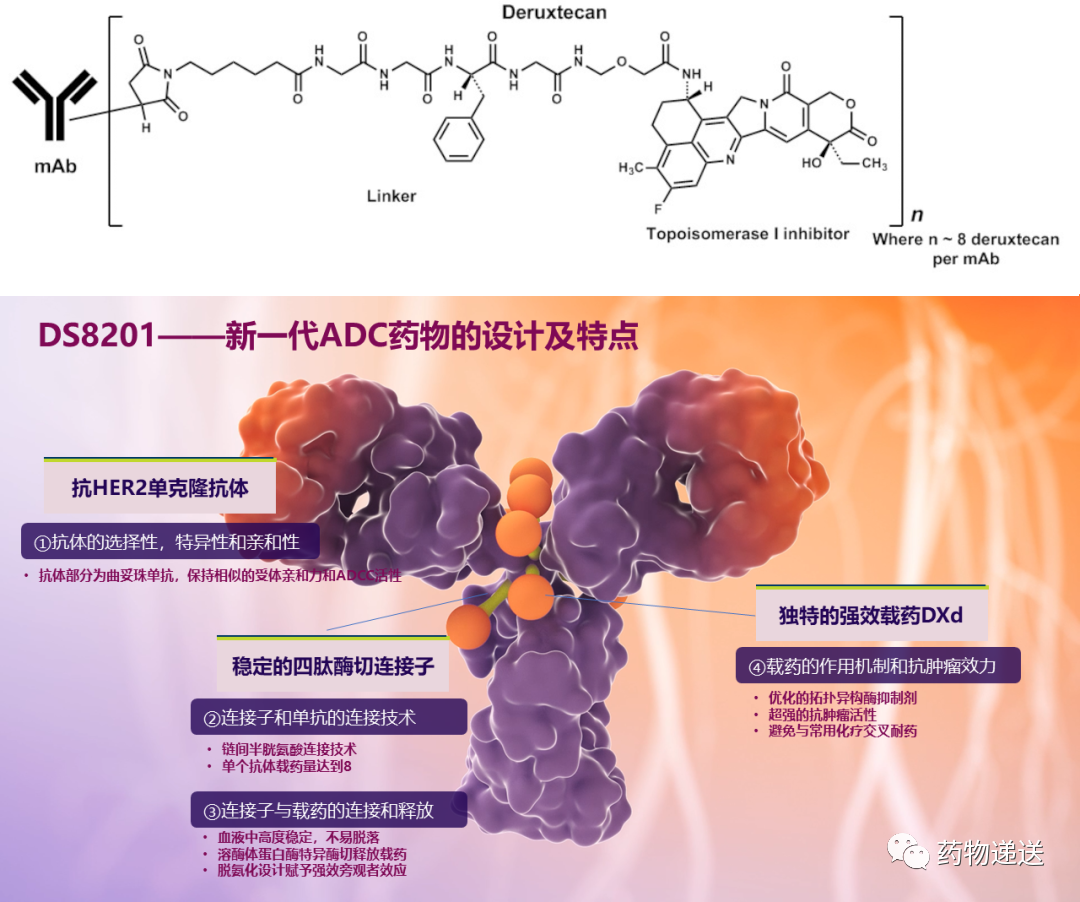
图7 DS-8201结构示意图及其特点
优化的连接子、独特的高活性载药、高DAR(Drugto Antibody Ratio,药物抗体比)以及强效旁观者效应,是DS-8201的最大特点。在DS-8201和恩美曲妥珠单抗T-DM1(trastuzumab emtansine)头对头对比中,相比T-DM1,DS-8201让患者病情进展的风险降低了72%,让患者死亡风险降低了45%。
DS-8201在2016年12月被FDA授予药物快速审核资格,于2019年12月20日加速批准其用于治疗无法切除或转移性HER2阳性乳腺癌。2020年3月在日本获批晚期乳腺癌后线治疗适应证,5月在美国获得HER2阳性转移性胃癌和HER2阳性转移性非小细胞肺癌的突破性治疗批复,9月在日本获批HER2阳性转移性胃癌后线治疗适应证。2022年3月21日,DS-8201在国内提交了新药上市申请。
图8 DS-8201(Enhertu)
以胶束递送喜树碱药物的的案例是NK012,由NipponKayaku公司开发包载SN-38的聚合物胶束。该产品采用的聚合物材料为PEG12000-b-P(Glu) 7000,SN-38与聚谷氨酸通过共价结合包载药物,胶束的粒径为20nm,载药量为20%。
在临床II期研究中,NK012用于治疗接受过顺铂化疗的不可切除、复发性或转移性结肠直肠癌,每3周给药一次。目前,NK012正在美国进行用于治疗复发性小细胞肺癌和三阴性乳腺癌的临床II期研究。同时,为改善单一疗法,进一步提高疗效,也在研究NK012与5-氟尿嘧啶或者顺铂联合治疗小细胞肺癌。
澳大利亚的Starpharma公司深耕树枝状大分子多年,并开发了树枝状大分子包载和递送药物的技术平台DEP®,在该平台上有在研产品DEP®irinotecan,以树枝状大分子包载和递送伊立替康,临床应用中与Lynparza®(奥拉帕尼)联用治疗肿瘤。
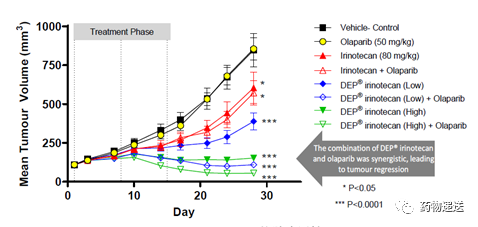
图9 DEP® irinotecan的抗肿瘤活性
药物递送技术是开发药物的有力工具,目前对于喜树碱药物的开发主要集中在伊立替康和SN-38上。希望在药物递送技术的助力下,能克服更多的喜树碱药物水溶性差、组织分布不足等缺点,开发出更多的抗肿瘤新药。
参考文献:
Camptothecin'sjourney from discovery to WHO Essential Medicine:Fiftyyears of promise
https://mp.weixin.qq.com/s/whbd906fppaA2LEJ4yrX3Q
https://mp.weixin.qq.com/s/IiX8fpsJfBgbo1Szo4oqig
喜树碱老兵新传
喜树碱类衍生物脂质体的研究进展
